Vrieskou onthult verrassende schakeling in ons immuunsysteem
ArrayOnderzoekers van de Universiteit Utrecht en het Leids Universitair Medisch Centrum hebben voor het eerst een van de belangrijke ‘aan-schakelaars’ van ons immuunsysteem in beeld gebracht. De hiervoor gebruikte nieuwe onderzoeksmethode leverde al direct een verrassend inzicht op. Zulke nieuwe inzichten kunnen gebruikt worden om betere behandelingen voor infecties en kanker te ontwikkelen, aldus onderzoeksleiders Piet Gros en Thom Sharp. De resultaten van het onderzoek zijn vrijdag 16 februari gepubliceerd in het wetenschappelijk tijdschrift Science.
Als in ons lichaam bacteriën, virussen of tumoren worden gesignaleerd, gaan onze immuun-eiwitten (antilichamen) onmiddellijk in de verdediging. Ze markeren deze afwijkende oppervlakken en waarschuwen het afweersysteem. Dit is het signaal voor verschillende eiwitmoleculen die samen het zogeheten C1-complex vormen, om het gevaar aan te vallen en te vernietigen. Het is dit belangrijke C1-complex dat nu in beeld is gebracht. Tot nu toe was niet bekend hoe dit complex precies indringers herkent en hoe het vervolgens geactiveerd wordt.
Onderzoek in natuurlijke omgeving
Het onderzoeken van het C1-complex is moeilijk, omdat de moleculen die het vormen buiten hun natuurlijke omgeving snel samenklonteren. De onderzoekers van de Universiteit Utrecht en het Leids Universitair Medisch Centrum zochten samen met het internationale biotech bedrijf Genmab A/S een manier om toch de activatie van het complex in een natuurgetrouwe omgeving te kunnen vastleggen. Hiervoor kwamen ze op een combinatie van twee beeldvormingstechnieken: cryo- elektronenmicroscopie (CryoEM) en cryo- elektronentomografie (CryoET).
Beeld ‘bevroren’
 Beide technieken worden uitgevoerd bij zeer lage temperaturen (cryo). Hierdoor wordt het ‘beeld’ even ‘bevroren’, zodat het kan worden vastgelegd. Deze combinatie blijkt nu inderdaad de manier om de details van ons immuunsysteem te analyseren.
Beide technieken worden uitgevoerd bij zeer lage temperaturen (cryo). Hierdoor wordt het ‘beeld’ even ‘bevroren’, zodat het kan worden vastgelegd. Deze combinatie blijkt nu inderdaad de manier om de details van ons immuunsysteem te analyseren.
Reconstructie tot 3D-structuur
Bij cryo-elektronenmicroscopie worden duizenden kopieën van het complex als het ware uitgestrooid over de kleefkant van een stukje plakband, waardoor ze allemaal in een net iets andere positie liggen. Vervolgens worden met een camera opnamen gemaakt vanuit één vaste positie. Bij cryo-elektronentomografie wordt het complex in beeld gebracht in een meer natuurlijke omgeving, alsof het gebonden is aan het celoppervlak. Net als bij een CT-scan, worden opnamen van het deeltje gemaakt terwijl het ronddraait, dus vanuit allemaal verschillende hoeken. In beide gevallen wordt uit alle beelden een driedimensionale structuur gereconstrueerd.
Nog gedetailleerder, levensecht beeld
“Het gebruik van deze onderzoekstechnieken neemt in het onderzoek een enorme vlucht”, vertelt prof. Thom Sharp van het Leids Universitair Medisch Centrum. “Elke methode geeft ons andere, maar complementaire informatie over hetzelfde complex. Door die te integreren, ontstaat een nog gedetailleerder, levensecht beeld van dit ingewikkelde moleculaire systeem.”
Verrassend inzicht: twee manieren van activering
De nieuwe onderzoeksmethode leverde al direct een verrassend nieuw inzicht op: er is niet één, maar er zijn twee manieren waarop het C1-complex geactiveerd wordt. Soms wordt door antilichamen eerst een beperkt aantal waarschuwingssignalen herkend. De ruimtelijke structuur van het C1-complex vervormt zich dan om deze te kunnen binden. Zo’n aanpassing van één enkel complex kan dan al voldoende zijn om de hele afweerreactie in gang te zetten. In andere situaties, als direct veel waarschuwingssignalen worden herkend, lijken C1-complexen elkaar te kunnen activeren, zoals bij een buurtwachtsysteem.
Het artikel Structures of C1-IgG1 provide insights into how danger pattern recognition activates complement’ is op 16 februari verschenen in Science. Dit onderzoek is medegefinancierd door de Nederlandse Organisatie voor Wetenschappelijk Onderzoek en de European Research Council.
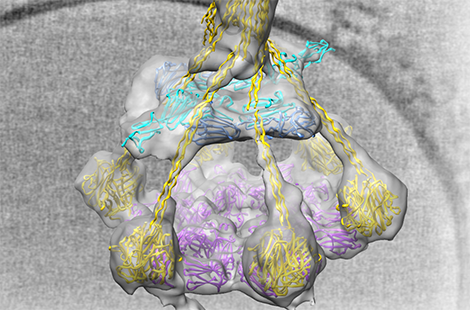
Beeld: Het C1-complex in 3D (in kleur) zoals het in de natuurgetrouwe omgeving is gebonden aan de antilichamen, vastgelegd met CryoEM en CryoET.
Bron: LUMC