 Array
ArraySlimmere geneesmiddelafgifte dankzij controle over bezorgpakketjes
Onderzoekers van de TU Eindhoven en de Universiteit Utrecht hebben de parameters ontdekt die de inkapseling in bezorgpakketjes van medicijnen bepalen. Dit geeft meer invloed over gestage afgifte van geneesmiddelen bij patiënten. Bovendien zal het ontwerpen van inkapselingen voor nieuwe geneesmiddelen nu veel minder experimenten vergen, wat een snellere en goedkopere ontwikkeling van geneesmiddelen mogelijk maakt. De onderzoekers geloven dat dit werk een belangrijke impact zal hebben op het biomedische veld en het ontwerpen van toekomstige geneesmiddelen.
Hydrofoob
Veel geneesmiddelen zijn hydrofoob — ze lossen niet goed op in water — waardoor de toediening van geneesmiddelen bij patiënten problematisch is. Een mogelijke oplossing is om de medicijnen in kleine verpakkingen in te kapselen die hydrofoob (waterafstotend) zijn aan de binnenkant en hydrofiel (wateroplosbaar) aan de buitenkant. De geneesmiddelen hopen zich op in de binnenkant van deze verpakkingen en het transport van het geneesmiddel door het lichaam van de patiënt wordt veel gemakkelijker.
De verpakkingen bestaan vaak uit bijbehorende oppervlakte-actieve stoffen, die al goedgekeurd zijn in de farmaceutische industrie. Wanneer opgelost in water, een fysiologische oplossing, of bloed, oriënteren de verpakkingsmoleculen hun hydrofobe deel naar de binnenste kern (met affiniteit voor de onoplosbare geneesmiddelen) en hun hydrofiele kant naar buiten toe, en vormen zo een bolvormig ‘pakket’, een zogenaamde micel.
De verblijfplaats in een micel
Het is al tientallen jaren mogelijk om geneesmiddelen op deze manier door het hele lichaam te vervoeren, maar pas nu begrijpen onderzoekers welke factoren precies bepalen waar geneesmiddelen zich in de micel verzamelen. Deze ruimtelijke spreiding kan een dramatische invloed hebben op de afgifte van de geneesmiddelen in een patiënt. Sommige geneesmiddelen concentreren zich in het midden van de hydrofobe kern van de micel en komen langzaam vrij. Dat is erg wenselijk voor de opname van geneesmiddelen door een patiënt. Andere geneesmiddelen verzamelen zich bij de kern van de micel en komen meestal sneller vrij. Daarom is het beheersen van de locatie van het geneesmiddel in de micel belangrijk voor de afgiftesnelheid van de geneesmiddelen.
Een kleurstof om een geneesmiddel op te volgen
Om te onderzoeken waar onoplosbare geneesmiddelen zich verzamelen, gebruikten de onderzoekers Nijlrood, een kleurstofmolecuul dat lijkt in grootte en oplosbaarheid op typische geneesmiddelen. De kleurstof heeft een handige eigenschap: niet alleen absorbeert het een specifieke kleur licht, maar ook is die kleur afhankelijk van diens omgeving. Als de kleurstof is opgelost in zuiver water, absorbeert een andere kleur licht dan als er ook wat alcohol in het water is opgelost.
Om te onderzoeken waar onoplosbare geneesmiddelen zich verzamelen, gebruikten de onderzoekers Nijlrood, een kleurstofmolecuul dat lijkt in grootte en oplosbaarheid op typische geneesmiddelen. De kleurstof heeft een handige eigenschap: niet alleen absorbeert het een specifieke kleur licht, maar ook is die kleur afhankelijk van diens omgeving. Als de kleurstof is opgelost in zuiver water, absorbeert een andere kleur licht dan als er ook wat alcohol in het water is opgelost.
Het veranderen van de water/alcohol-verhouding is een slimme manier om een goed oplosmiddel of een slecht oplosmiddel voor de kleurstof te simuleren. Dit is analoog aan het werken met een wateroplosbaar medicijn of een dat niet oplost. Door de lichtabsorptie te meten, konden de onderzoekers bepalen hoeveel kleurstof zich in de kern van de micel verzamelt en hoeveel op het raakvlak tussen de kern en de schil van het medicijnpakketje
Experimenten gecombineerd met computersimulaties
Om hun bevindingen te bevestigen, hebben de onderzoekers computersimulaties gedaan. Daarmee bepaalden ze zowel de locatie van de opgeloste medicijnmoleculen en de vorm van de blok co-polymeer-micel. De berekeningen onthullen de ordening van de componenten binnen en buiten de micel, waardoor de voorkeurgebieden van het geneesmiddel konden worden bepaald.
Uit de experimenten en berekeningen werd geconcludeerd dat het gewenste gebied van het geneesmiddel in de blok co-polymeer-micellen vooral wordt bepaald door de concentratie en de oplosbaarheid van de geneesmiddelenmoleculen in het omringende medium (water/fysiologisch medium/bloed). Als de concentratie van het geneesmiddel onder de maximale oplosbaarheid van het oplosmiddel ligt, verzamelen de geneesmiddelenmoleculen zich bij het grensgebied tussen de kern en schil van de micel, terwijl ze zich bij een concentratie boven de maximale oplosbaarheid juist binnenin de kern verzamelen.
Beter doordachte medicijnontwikkeling
Het huidige onderzoek naar inkapseling van geneesmiddelen wordt bestaat veel door trial-and-error-experimenten. De resultaten van het Eindhovense onderzoek maken eenvoudigere en goedkopere ontwikkeling van ‘smart drugs’ mogelijk. Dit zal helpen om de bijwerkingen van medicatie te verminderen en de ontwikkeling van gepersonaliseerde medicatie te vergemakkelijken. Hierbij wordt de afgifte van het geneesmiddel specifiek aangepast aan de individuele behoeften van de patiënt.
Referentie wetenschappelijke publicatie
“Controlling the spatial distribution of solubilized compounds within copolymer micelles”, Alessandro Ianiro, Álvaro González García, Stefan Wijker, Joseph P. Patterson, A. Catarina C. Esteves, en Remco Tuinier Langmuir DOI:10.1021/acs.langmuir.9b00180
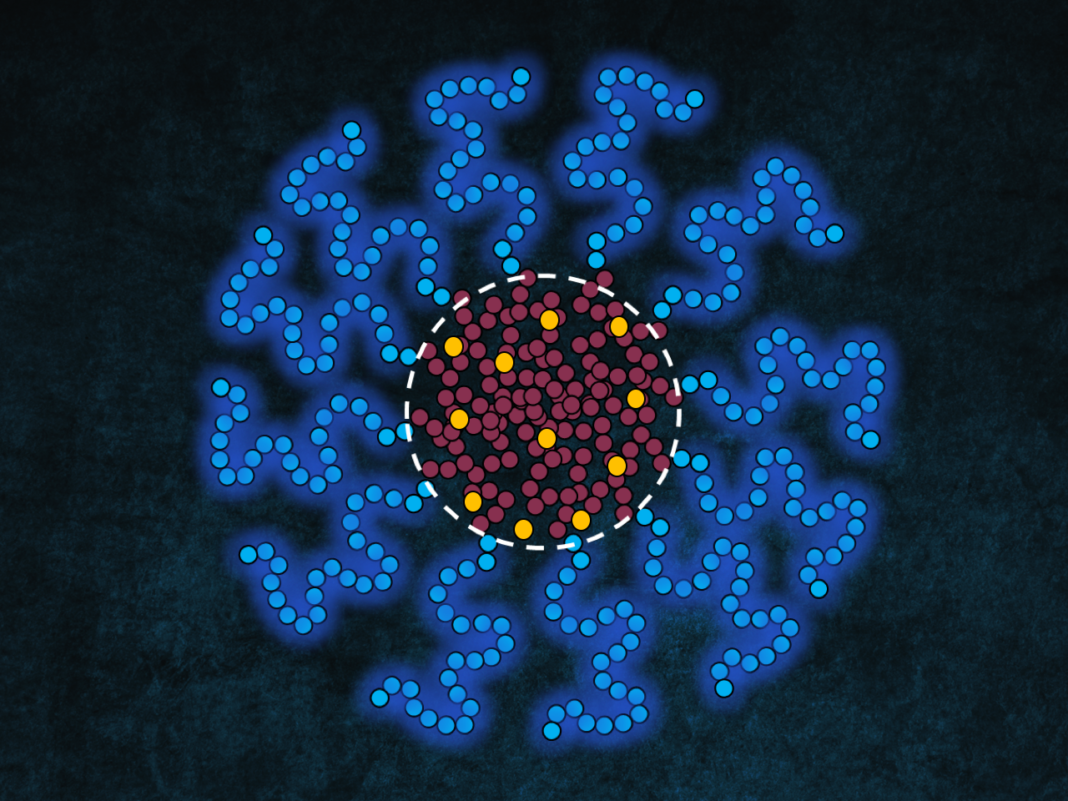
Schematische afbeelding van een micel die bestaat uit een hydrofiele schil (blauwe ketens) en een hydrofobe kern (rode ketens) die medicijnmoleculen (geel) inkapst. De medicijnmoleculen verzamelen zich meestal op het raakvlak van de kern en schil van de micel (witte stippellijn) als de concentratie van het geneesmiddel zich onder de maximale oplosbaarheid van het oplosmiddel bevindt, terwijl ze zich bij een concentratie boven de oplosbaarheid in de kern verzamelen. (Afbeelding: Alessandro Ianori)
Bron: TU/e Eindhoven